Знаете, откуда появляются дети? Клинические эмбриологи сказали бы, что из чашек Петри. О том, как происходит чудо зарождения жизни и зачем делать ЭКО рыбам, мы расспросили Дарью Свистунову — научную сотрудницу Института биологии гена РАН, которая предпочла науку клинике.
«В аспирантуре я придумывала эксперименты во сне и очень расстраивалась, когда наутро не могла их вспомнить»
Я окончила факультет биоинженерии и биоинформатики (ФББ) МГУ с красным дипломом. Потом поступила в Оксфордский университет в магистратуру по клинической эмбриологии. Эмбриологию я выбрала, потому что это был единственный экзамен, после которого я второй раз прочитала учебник — для себя. В России этому особо не учили: на ФББ был очень абстрактный полугодовой курс.

Меня в науке в принципе тянет к вещам, которые находятся на грани загадок и этики, — а в эмбриологии мы буквально работаем с началом жизни. Когда я думала, куда идти в аспирантуру, нашла лабораторию, которая занималась прионными[1] заболеваниями. Но мама сказала, что это очень опасная работа: куда-нибудь в себя тыкну — и до свидания. Поэтому в аспирантуре я занималась нейродегенерацией на молекулярном уровне.
Самая смешная лажа в аспирантуре, которая у меня была в лаборатории, началась с того, что я должна была выделить РНК из мозгов. Я достаю их из морозилки, а они прилипли к Эппендорфу[2]
Беру пинцет, хватаю мозг с двух боков, пытаюсь выдернуть, и он у меня падает на пол. А мне кажется, пол в этой лаборатории никто не мыл примерно с момента открытия. Решила все-таки поставить ПЦР[3], уже понимая, что кривая там будет ужасная. Я его поднимаю, кладу в пробирку… И снова роняю на пол. Самый прикол, что кривая была идеальная, я даже не смогла определить, какой из образцов лежал на полу.
Еще я должна была рассадить первичные нейроны гиппокампа. Чтобы это сделать, нужно посчитать, в какой концентрации их посадить. На следующий день смотрю — клетки очень редко сидят. Оказалось, что я на порядок ошиблась. Значит, заглядываю в мусорку, которая стоит рядом с ламинаром[4], а там лежит фалькон[5] с клетками, которые я вчера сажала. Думаю: «Всё равно эксперимент уже не получится». Я их тряхнула, сняла со стенок, рассадила. Эксперимент особо не получился, но это неважно, зато я рассадила клетки из мусорки. У студентов всегда все валится из рук, но без такого опыта невозможно стать ученым. Зато в клинике я стала крайне аккуратной и внимательной — проверяла фамилию пациентки по 10 раз, прежде чем что-то сделать с клетками и эмбрионами.
Мне очень нравилась наука, но не нравилось пересаживать клетки в субботу в час ночи. Вот как-то совсем не мое. Поэтому я решила, что хочу работу, которую невозможно взять на дом, и в январе 2020-го устроилась в клинику ЭКО в Москве, когда уже набралась опыта в аспирантуре. Там я довольно быстро всему научилась из-за огромного потока пациентов: 1200–1300 свежих протоколов в год. Ты уже к концу дня забываешь фамилии пациенток, но зато очень быстро набиваешь руку.
В клинике здорово, что ты видишь результат своей работы: что-то поделал — и родился ребенок, вот его фотография
Но при этом очень скучно, когда не над чем поломать мозг. В аспирантуре я придумывала эксперименты во сне и очень расстраивалась, когда наутро не могла вспомнить, какой эксперимент ставила. А в клинике этого нет: твое дело — оплодотворять.
Бывали ситуации, когда приходила пациентка эдакая, со сложной генетикой. Я пыталась заинтересовать коллег: вот бы посмотреть, какая там мутация, а вот почитайте статейку на PubMed'е. А мне говорили: «Даш, иди оплодотворяй». Становилось немного обидно, но в реальности мы не можем сказать пациентке: «Ой, а вы не могли бы геномчик за 150 тысяч сдать, а мы посмотрим, что у вас там интересного, а дальше всё равно предложим каталог донорских ооцитов[6]». Да, мы разгадаем эту научную загадку, но это никак не поможет пациентке.

У нас была история: первичное бесплодие, у мужа хорошая сперма, мы получили много клеток и решили поставить ЭКО. На следующий день приходим проверять, а там только две правильно оплодотворенные яйцеклетки. А остальные содержат три-пять гаплоидных[7] наборов. Мы перенесли пациентке то, что выросло нормально, но беременности не случилось, что неудивительно, потому что эмбрион был так себе. Потом она пришла снова. Мы решили делать ИКСИ[8]: берешь один сперматозоид, ломаешь ему хвост и вводишь прямо в ооцит. Таким образом мы исключаем оплодотворение несколькими сперматозоидами. На следующий день та же история, что в прошлый раз. Невозможность решить такие загадки очень демотивирует, особенно когда видишь потенциальную статью, которую не можешь написать.
«Если мы вылечили рыбу, то это не значит, что мы вылечим Альцгеймер»
Именно поэтому я вернулась назад в науку. Я уже смирилась с тем, что мне надо писать статьи, потому что я теперь взрослая: уже ручками достаточно поработала в аспирантуре. Основной проект, который я веду, заключается в исследовании семейства генов TLDс. В этом семействе пять канонических генов: три изучены нормально, один — кое-как, один — примерно никак. Три самых изученных экспрессируются в центральной нервной системе, а мутации — это глухота, эпилепсия, микроцефалия, нейродегенерация, дегенерация мозжечка и расстройство аутистического спектра.
Мыши с нокаутом гена[9] OXR1 рождаются нормальными, но на 18-й день у них начинает развиваться фенотип — гибель гранулярных мозжечковых нейронов, на 25–26-й день жизни они погибают от атаксии и потери веса. При этом мыши с нокаутом другого гена (NCOA7) живут долго и счастливо, у них только pH мочи нарушен и снижена фертильность. Мы в лаборатории занимаемся генным редактированием рыбулек, потому что это очень удобный модельный организм: если у мыши помет 5–6 мышат, то у рыбы — 200 икринок. По сути, ты сразу делаешь репрезентативную выборку. Кроме того, на рыбах удобно изучать эмбриогенез, потому что его буквально видно.
На рыбах можно смоделировать мутацию в гене нашего интереса, которая была описана у человека с конкретным генотипом, сравнить фенотипы и дальше эту рыбу вдоль и поперек вскрывать, заливать какими-нибудь веществами и тестировать лекарства. Но, безусловно, если мы вылечили рыбу, то это не значит, что мы вылечим Альцгеймер. Так оно, к сожалению, не работает. Когда-нибудь, наверное, всё можно будет масштабировать на человека, но пока мы изучаем рыбулек.
«Бывало, что переносишь нечто косое, кривое, непонятное, а в итоге — беременность и роды»
По сути клиническая эмбриология — это та же работа в лабе. Сначала пациенты консультируются с репродуктологом и проходят все обследования. Женщинам назначается гормональная стимуляция: каждый день она делает себе уколы, чтобы за один цикл выросло много фолликулов. У каждой женщины разный овариальный резерв, поэтому созревает разное количество фолликулов, обычно у женщин 30–35 лет это 15–20 клеточек. Максимальная моя пункция была 60 фолликулов, но это уже слишком много — женщина была донором ооцитов. Когда врач решает, что их необходимо пунктировать, назначается укол, который стимулирует дозревание яйцеклеток, потому что в норме они находятся в мейоз-аресте[10].
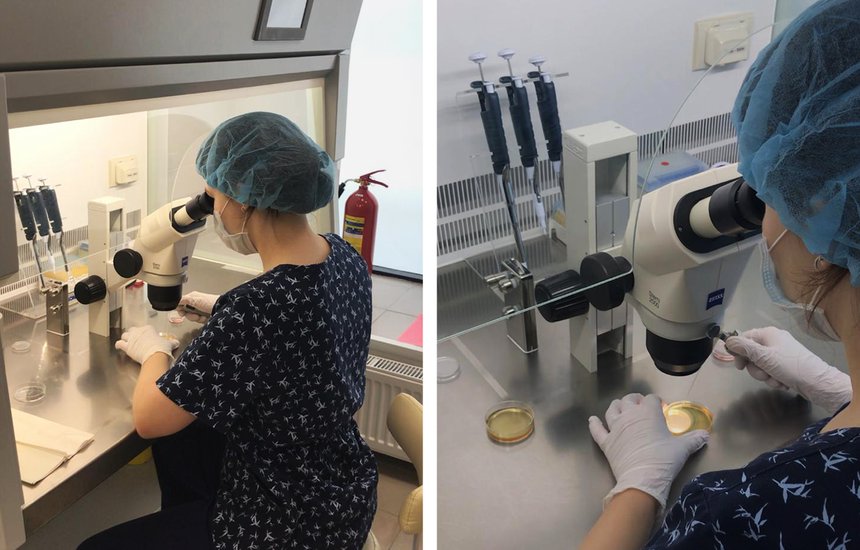
Затем назначается трансвагинальная пункция фолликулов, которая в 99% случаев проводится под наркозом. Женщина лежит в операционной на гинекологическом кресле, а врач с помощью датчика УЗИ и длиннющей 30-сантиметровой иглы входит в фолликул и аспирирует его в пробирочку. Тут включается эмбриолог, который содержимое этой пробирки выливает в чашку Петри и оценивает под микроскопом наличие клеток, которые потом отправляются в инкубатор. В зависимости от технологии — ИКСИ или ЭКО — клетки чистятся от кумулюса[11] или нет.
Параллельно с пункцией сдается мужчина. Мы смотрим спермограмму в день оплодотворения, потому что случается, что переживания снижают показатели. Если всё в порядке, то через три часа мы оплодотворяем яйцеклетки методом ЭКО — смешиваем в лунке кучу яйцеклеток со сперматозоидами. На следующий день мы смотрим, кто оплодотворился: убираем оставшиеся клетки кумулюса и смотрим на количество пронуклеусов[12]: 2pn, 3pn или 0pn, если клетка не оплодотворилась.
Чаще всего эмбрионы растят до пятого дня — стадии бластоцисты[13]. Это именно та стадия, на которой эмбрион достигает матки, если мы говорим про естественный процесс, и готов к процессу имплантации. Если эмбрион немного отстает, то мы ему можем дать время до следующего дня — до шестых суток. Вообще, нам не жалко, пусть стоит, но если видим, что он остановился в развитии на стадии 5–6 клеток, то списываем.
Мы оцениваем качество бластоцист по определенным метрикам. Конечно, пациентам мы говорим просто «хорошая», «отличная» или «бесперспективная». Слово «плохой» я старалась не говорить. Ты никогда не знаешь, а вдруг это тот самый эмбрион? Бывает, что выросло десять клеток, две бластоцисты — одна другой страшнее, но тебе больше не с чем работать. Поэтому ты говоришь: «Эмбрионы качества не очень, но мы попробуем перенести». Да, у них снижены шансы на имплантацию относительно эмбрионов хорошего качества, но мы даем им шанс, потому что во время развития в матке на них воздействуют различные факторы, выделяемые клетками эндометрия, которые могут помочь развиться этим эмбрионам в лучшее качество и имплантироваться. Мне кажется, здесь все-таки присутствует психосоматический фактор тоже. Иногда реально бывало, что переносишь нечто косое, кривое, непонятное, а в итоге — беременность и роды. А переносишь что-то красивое — и ничего положительного нет. Какая-то вера тоже играет роль. Хотя я же за науку — тогда это эпигенетика[14].

Мы не несем ответственности за то, приживется эмбрион или нет, это всё воля случая. Перенос осуществляет репродуктолог, мы только должны правильно набрать эмбрион в катетер, больше ни на что повлиять не можем. Даже на ЭКО случается внематочная беременность, мало ли куда эмбрион заплыл. Случайные факторы исключать нельзя.
Считается, что при криопереносе шанс наступления беременности выше. В свежем протоколе женщина после гормональной стимуляции, она там себя во все места колола. Это как минимум стресс и лишние гормоны, которых в норме быть не должно. А в криопротоколе женщине дают минимальное количество препаратов, просто чтобы лучше вырос эндометрий. А иногда это вообще делается в естественном цикле.
«Этическая дилемма эмбриолога заключается в том, чтобы не осуждать некоторых пациентов»
Я сама верю в науку и статистику. Случались глубоко религиозные пациентки, которые давали согласие на оплодотворение только двух-трех ооцитов, потому что православная церковь запрещает замораживать эмбрионы. То есть мы получили 10 клеток, семь заморозили, три оплодотворили, и всех эмбрионов, которые вырастают, по идее, мы должны перенести. С точки зрения медицины это опасно — возрастает вероятность многоплодной беременности. С точки зрения технологии это неразумно — эмбрионы хранятся гораздо лучше, чем яйцеклетки. Многие пациенты близко к сердцу принимают даже свои незрелые клетки, которые при всем желании не смогут стать эмбрионами: как ее утилизировать, если это родненькая клеточка. Наверное, в теории можно забрать свою яйцеклетку домой, потому что материал же не наш. Но проблема в том, что дома в холодильнике это нельзя хранить, только в жидком азоте. Правда, я с такими запросами не сталкивалась.
Говорят, что мы играем в Бога, но это не так. Если наверху кто-то есть, то извлеченная яйцеклетка просто не оплодотворится
Эмбрион плохого качества, который не сможет имплантироваться, мы утилизируем. От того, что я его выкину, я не поменяю его судьбу. Но при этом очень жалко, когда пациенты отказываются от криоконсервации действительно хороших эмбрионов. Тут сердце кровью обливается, но я же не могу заморозить его себе на память. Могу только многочисленными попытками переубедить. Если получаю стойкое «нет», то потом думаю: «А зачем приходить на ЭКО тогда, если ты не хочешь заморозить свой шикарный эмбрион?» Этическая дилемма эмбриолога скорее заключается в том, чтобы не осуждать некоторых пациентов. Если замороженные эмбрионы не пригодились, то их можно подсадить другому человеку, если подписано согласие на донорство. А если нет, то они бесконечно хранятся, просто лежат и лежат.
Эмбриология как индустрия регламентируется 803-м приказом Минздрава РФ. Там прописано, кому положено ЭКО, как должны обследоваться доноры, что мы должны вести многочисленные журналы, которые зачастую дублируют друг друга. Например, там фиксируется, что не допускается перенос более двух эмбрионов. На заре ЭКО могли перенести по три-четыре эмбриона, как результат — многоплодные беременности, редукции и недоношенные тройни с ДЦП. Сейчас поле деятельности для косяков сократилось. Это радует.
Яйцеклетки и сперматозоиды для нас — просто клетки, как эритроциты, клетки кожи и тому подобное. Со сперматозоидами мы можем ругаться, когда они от нас убегают, с яйцеклетками особо не поговоришь. К эмбрионам же другое отношение, особенно если он очень красивенький или ты сам делал ему биопсию. Если переносим эмбрион, который выглядит средненько, а он единственный у пациентки, то говорим ему: «Давай, давай, дружочек». Мы за них переживаем.
Обычно эмбриологи видят пациенток под особым ракурсом — это лежащая в кресле женщина под наркозом, которую в коридоре в лицо не узнаешь. Но если у пациентки особая история, например много выкидышей, то ты сердцем прикипаешь и хочешь, чтобы у нее всё получилось.
«Лучше знать сейчас, что яйцеклеток мало, чем потом листать каталог доноров»
У хороших эмбрионов на пятый день есть три потенциальные судьбы. Мы можем их перенести — это свежий перенос, дальше ждем 14 дней, и женщина сдает анализ на ХГЧ (хорионический гонадотропин человека). Второй путь — криоконсервация: если выросла куча эмбрионов, остальные не выкидывать же. А третий вариант — мы можем эти эмбрионы пробиопсировать и потом уже заморозить. Это необходимо, если у женщины есть какие-то показания к генетическому тестированию (ПГТ): возрастной фактор или носительство моногенного заболевания.
С возрастом у женщин естественным образом возрастают риски анеуплоидии[15]. Еще у женщин старшего репродуктивного возраста (39 лет) выше риск, например, родить ребенка с синдромом Дауна. Это происходит из-за того, что яйцеклетка находится в аресте мейоза с момента рождения: веретена хромосом в ней физически растянуты к полюсам. Эти клетки очень долго ждут, поэтому веретена могут рушиться. Следовательно, чем старше женщина, тем выше вероятность, что яйцеклетка будет нести неправильное число хромосом. На моей памяти самая старшая пациентка со свежим переносом собственных клеток — 44 года, с донорскими ооцитами — 54 года, беременность наступила, но про роды информации нет.
Если есть подозрение на моногенное заболевание, то нам нужно знать, что искать. То есть нельзя просто прийти и сказать: «А вы мне, пожалуйста, проверьте на всё». Так это не работает. Родители должны заранее сдать генетический тест. Например, они оба носители генетической вариации, которая кодирует муковисцидоз. Соответственно, мы тогда знаем, что должны проверять эмбрионы на муковисцидоз. Но это не исключает того, что у эмбриона окажется нейросенсорная тугоухость. Смотрим, правда, не мы, конечно же: мы делаем биопсию, замораживаем образец и отправляем в генетическую лабораторию.
Генетическое тестирование можно провести на все моногенные заболевания. Это заболевания, в отношении которых мы знаем, что мутация в конкретном гене приводит к конкретному заболеванию. Например, муковисцидоз, гемофилия, тугоухость, фенилкетонурия. На болезнь Альцгеймера протестировать невозможно, потому что мы не знаем, с какой мутацией она связана. Есть отдельные наследственные случаи, описанные в литературе, но это скорее редкость. У меня как-то были пациенты, которые планировали суррогатное материнство по показаниям, то есть у семьи были деньги, я в таких случаях всегда предлагаю посмотреть расширенную генетику. Они сказали, что хотели бы проверить на аутизм. Тут история как с болезнью Альцгеймера: определенного гена, который нам точно бы сказал, будет ли аутизм, нет. Есть только гены-кандидаты, изменения в которых могут повышать риск возникновения аутизма. Если в семье были случаи аутизма, то есть возможность поискать этот ген в геноме родственников. Но опять-таки далеко не факт, что мы найдем генетическую причину. На всё остальное они проверяться отказались.
По закону выбирать пол ребенка запрещено, если нет показаний в виде генетических заболеваний, которые наследуются с полом. Но на бланках ПГТ, которые выдаются пациентам на руки, указаны половые хромосомы: не нужно быть гением, чтобы понять, что к чему. Без биопсии мы пол ребенка не увидим. Меня иногда спрашивают пациенты, у которых свежий перенос: «А вы не знаете, там мальчик или девочка?» А это всё выглядит как елочный шарик. Бантика розового или голубого там нет.
Я большой любитель генетики, поэтому всегда советую сдавать анализы: лучше потратить 100 тысяч на анализ, чем потом лечить больного ребенка или пережить внутриутробную гибель плода. Еще советую всем женщинам сдать анализ на АМГ (антимюллеров гормон), потому что лучше знать сейчас, что яйцеклеток мало, чем потом листать каталог доноров. Я тоже сдавала генетический тест, но безотносительно беременности. Просто подумала, а почему бы не сдать экзомчик. И узнала, что я носитель нескольких заболеваний, но крайне редких. Если я буду планировать новую беременность, то хотела бы, чтобы мой партнер тоже сдал этот анализ. Однако грустная вещь в том, что сейчас в статьях описаны случаи, когда один родитель — носитель заболевания, а второй не имеет мутации, но ребенок всё равно приобретает патогенный фенотип, потому что мутация возникает de novo. Но такие случаи — большая редкость, а от большинства заболеваний можно уберечься. Не нужно думать, что если у вас в семье все здоровы, то однозначно не может родиться больной ребенок.
Обложка: © Rohane Hamilton / Shutterstock / Fotodom